دوره 33، شماره 2 - ( 4-1403 )
جلد 33 شماره 2 صفحات 239-228 |
برگشت به فهرست نسخه ها
Research code: IRCT20230430058033N1
Ethics code: IR.BASU.REC.1401.026
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Yalfani A, Asgarpoor A. Investigating the Effects of Neurofeedback Training on Psychological Variables in Women With Non-specific Chronic Back Pain: A Randomized Controlled Trial. JGUMS 2024; 33 (2) :228-239
URL: http://journal.gums.ac.ir/article-1-2654-fa.html
URL: http://journal.gums.ac.ir/article-1-2654-fa.html
یلفانی علی، عسگرپور آزاده. تأثیر تمرین نوروفیدبک بر متغیرهای روانشناختی زنان مبتلا به کمردرد مزمن غیراختصاصی: یک کارآزمایی بالینی کنترلشده تصادفی. مجله علوم پزشکی گیلان. 1403; 33 (2) :228-239
علی یلفانی*1 

 ، آزاده عسگرپور1
، آزاده عسگرپور1 




 ، آزاده عسگرپور1
، آزاده عسگرپور1 


1- گروه آسیبشناسی و حرکات اصلاحی، دانشکده تربیتبدنی و علوم ورزشی، دانشگاه بوعلی سینا، همدان، ایران.
متن کامل [PDF 4075 kb]
(454 دریافت)
| چکیده (HTML) (1715 مشاهده)
متن کامل: (766 مشاهده)
مقدمه
کمردرد مزمن در سراسر جهان یکی از مهمترین مسائل پزشکی ازلحاظ کاهش کیفیت زندگی، ناتوانی و افزایش هزینههای اجتماعی و اقتصادی است [1]. بهطورکلی کمردرد در 2 دسته غیراختصاصی و مکانیکی طبقهبندی میشود. کمردرد مزمن غیراختصاصی 90 الی 95 درصد از کمردردها را شامل میشود و 20 درصد از جمعیت جهان را تحت تأثیر قرار میدهد [2 ,3]. کمردرد مزمن غیراختصاصی یک بیماری پیچیده و پاتوفیزیولوژی آن ناشناخته است که در مدت 3 ماه یا فراتر رخ میدهد [4]. شواهد قوی وجود دارد که نشان میدهد کمردرد با تعامل پیچیدهای از عوامل شناختی [5]، فیزیکی [6]، روانی [7]، نوروفیزیولوژیک [7] و سبک زندگی [8] مرتبط است. اگرچه بسیاری از این عوامل بهطور بالقوه قابلتغییر هستند، اغلب، پروتکلهای توانبخشی کمردرد مزمن بر مداخلات فیزیکی متمرکز است [9]. مداخلات فیزیکی ممکن است بر عوامل روانی تأثیری نداشته باشند [10].
عوامل روانشناختی نهتنها فعالیت قشر پردازش درد را تغییر میدهند، بلکه عملکرد مغز در قشر مربوط به توجه، پیشبینی و ناحیه احساسی درد را نیز تغییر میدهند [11]. مطالعات تغییرات قابلتوجهی را در مناطق کنترل درد، شناختی و سنسوری موتور، مانند تالاموس و قشر حسیحرکتی در زنان مبتلا به کمردرد مزمن گزارش کردند [12]. با تغییر نوروفیزیولوژیک سیستم عصبی مرکزی، یکپارچگی حسی مختل شده [13] و با افزایش توجه به محرکهای دردناک، کنترل حرکتی بیماران مبتلا به کمردرد مزمن تغییر میکند [14]. بنابراین لازم است مکانیسمهای عصبی که باعث درد، ناتوانی، اختلال حرکتی و اختلال در عملکرد سیستم عصبی مرکزی میشوند، شناسایی شوند [11]. در این راستا، مطالعات تصویربرداری عصبی، تغییرات ساختاری و عملکردی مغز را در شرایط درد مزمن اسکلتیعضلانی نشان داد. بهعنوان مثال محققان تغییراتی را در مورفولوژی و عملکرد مغز در بیماران مبتلا به کمردرد مزمن در مقایسه با گروه کنترل بدون درد گزارش کردند [15-17]. مطالعات پیشین با استفاده از تصویربرداری مغناطیسی، مگنتوآنسفالوگرافی، نوروفیدبک [15] و تحریک مغناطیسی ترانس کرانیال، بر روی بیماران مبتلا به کمردرد مزمن کاهش قابلتوجهی در تراکم ماده خاکستری در نواحی پیشپیشانی و تالاموس [18] و همچنین تغییرات در قشر حرکتی اولیه و سوماتوسنسوری [12] را نشان دادهاند.
اخیراً، تمرینات نوروفیدبک نیز مورد توجه محققان قرار گرفته است، زیرا اطلاعات قابلاعتمادی درمورد عملکرد مغز در حین استراحت، تحریک حسی و وظایف شناختی ارائه میدهد. علاوهبراین، این روش ایمن، ارزان و غیرتهاجمی است و آن را به یک دستگاه ارزشمند برای کاربردهای بالینی و تحقیقاتی تبدیل کرده است [19, 20]. علیرغم کاربرد گسترده نوروفیدبک برای ارزیابی تغییرات قشر مغز در شرایط درد مزمن اسکلتیعضلانی، دانش نسبتاً کمی درمورد تغییرات فعالیت امواج مغزی در بیماران کمردرد مزمن وجود دارد. نتایج مطالعه مرور سیستماتیک گزارش کرده است که تجربه درد با فعالیت امواج مغزی در ارتباط است. بدینصورت که در افراد مبتلا به دردهای مزمن مانند دردهای مزمن اعصاب کمری، امواج آلفا کاهش و امواج بتا و تتا افزایش پیدا میکند [21, 22]. بررسیهای سیستماتیک و متاآنالیزهای اخیر نشان میدهد تمرینات نوروفیدبک با هدف مدولاسیون شبکههای عصبی بدون هیچگونه تحریک الکتریکی بر مغز، مزایای بالینی معنیداری در کاهش شدت درد در افراد مبتلا به درد مزمن ارائه میدهد [23-25]. همچنین چارمز و همکاران در مطالعه خود بیان کردند بیماران مبتلا به درد مزمن که برای کنترل فعالیت نسبی قشر قدامی (ناحیه مرتبط با درمان و تجربه درد) تحت درمان نوروفیدبک بودند، کاهش درد پس از جلسات تمرینی را گزارش کردهاند [26]. اگرچه یافتههای اولیه امیدوارکننده است، اما تعداد اندکی مطالعه درمورد تأثیر مداخلاتی که فعالیت مغزی در افراد مبتلا به درد مزمن اسکلتیعضلانی را تغییر میدهد منتشر شده و سؤالات بسیاری در این زمینه وجود دارد که از رایجترین سؤالات سازوکار اثربخشی این نوع تمرینات در کاهش درد و نحوه طراحی پروتکلهای درمانی است. بنابراین هدف از مطالعه حاضر بررسی تأثیر نوروفیدبک بر متغیرهای روانشناختی در زنان مبتلا به کمردرد مزمن غیراختصاصی بود. براساس شواهد مذکور فرض کردیم تمرینات نوروفیدبک به کاهش درد، ناتوانی و ترس از حرکت منجر خواهد شد. امید است نتایج مطالعه بینشی جدید و کاربردی جهت درمان کمردرد مزمن غیراختصاصی فراهم کند.
روشها
پژوهش حاضر از نوع کارآزمایی بالینی و طرح پژوهشی پیشآزمون پسآزمون با گروه کنترل بود. جامعه آماری این پژوهش شامل زنان با کمردرد مزمن غیراختصاصی است که از کلینیکهای ارتوپدی یا پزشکی ورزشی استان همدان انتخاب شدند. از نرمافزار جیپاور نسخه 3/1/9/2 برای تخمین حجم نمونه استفاده شد. خروجی نرمافزار 30 نفر را گزارش کرد. با در نظر گرفتن ریزش 10 درصد برای 40 بیمار برنامهریزی شد. 40 نفر از بیماران مذکور بهصورت هدفمند انتخابشده و بهصورت تصادفی به 2 گروه آزمایش و کنترل (هر گروه 20 نفر) تقسیم شدند. معیارهای ورود: سابقه درد بیش از 12 هفته، نداشتن سابقه جراحی ستون فقرات و تعویض مفصل ران و دامنه سنی بین 30 الی 50 سال. معیارهای خروج: درد در سایر سگمنتال بدن، دفورمیتی شدید اندام تحتانی و فوقانی، سابقه جراحی، استفاده از داروهای ضددرد طی 6 ماه گذشته، فیزیوتراپی در 1 سال گذشته، شرکت در ورزش، درد سیاتیک، اسپاندیلولیز، اختلالات عصبیعضلانی، نورولوژیکی، تنفسی، اسپاسم عضلانی و شکستگی مهرهها. بیماران قبل از جمعآوری اطلاعات رضایتنامه آگاهانه را امضا کردند.
ارزیابیها
مقیاس بصری سنجش درد
درد با مقیاس آنالوگ بصری، 10 سانتیمتری ارزیابی شد. از بیمار خواسته شد که شدت درد را در طول فعالیتهای روزانه نشان دهد [27].
ناتوانی
شاخص ناتوانی اوسستوری برای ارزیابی ناتوانی استفاده شد (ICC=0/84) [28]. این شاخص 10 آیتم دارد و هر آیتم از 6 زیرمجموعه تشکیل شده است. درمجموع، میزان ناتوانی در 4 زیرمجموعه طبقهبندی میشود: امتیاز کمتر از 25 بهعنوان پایینترین سطح ناتوانی، امتیاز 25 الی50 بهعنوان ناتوانی متوسط، نمره 50 تا 75 بهعنوان ناتوانی شدید و نمره 75 تا 100 بهعنوان ناتوانی حاد [29].
کنزیوفوبیا
ترس از حرکت توسط مقیاس تامپا سنجیده شد. این پرسشنامه دارای 11 عبارت است. از آزمودنی خواسته شد تا هریک از عبارات را براساس احساس واقعی خود تکمیل کند و هدف آن ارزیابی میزان ترس از حرکت از ابعاد مختلف (باور به آسیبدیدگی، اجتناب از فعالیت) بود. طیف نمرهگذاری آن براساس طیف لیکرت 4 گزینهای ( به گزینه کاملاً مخالفم نمره 1 و به گزینه کاملاً موافقم نمره 4 تعلق میگیرد) بود [30].
مداخله نوروفیدبک
برای اجرای مداخله درمانی نوروفیدبک و ثبت بازخورد در این مطالعه، از دستگاه 8 کانالProcomp Infinity ساخت شرکت Toget Technology کانادا استفاده شد. این دستگاه دارای سختافزار Procomp و نرمافزار Biograph Infinity نسخه 5 است. لوازم جانبی دستگاه شامل سنسور امواج مغزی، سه الکترود: الکترود فعال(آبی)، الکترود مرجع (زرد)، الکترود زمین (مشکی)، تقویتکننده، واحد رابط TT-USB، کابل فیبر نوری و کابل USB بود.
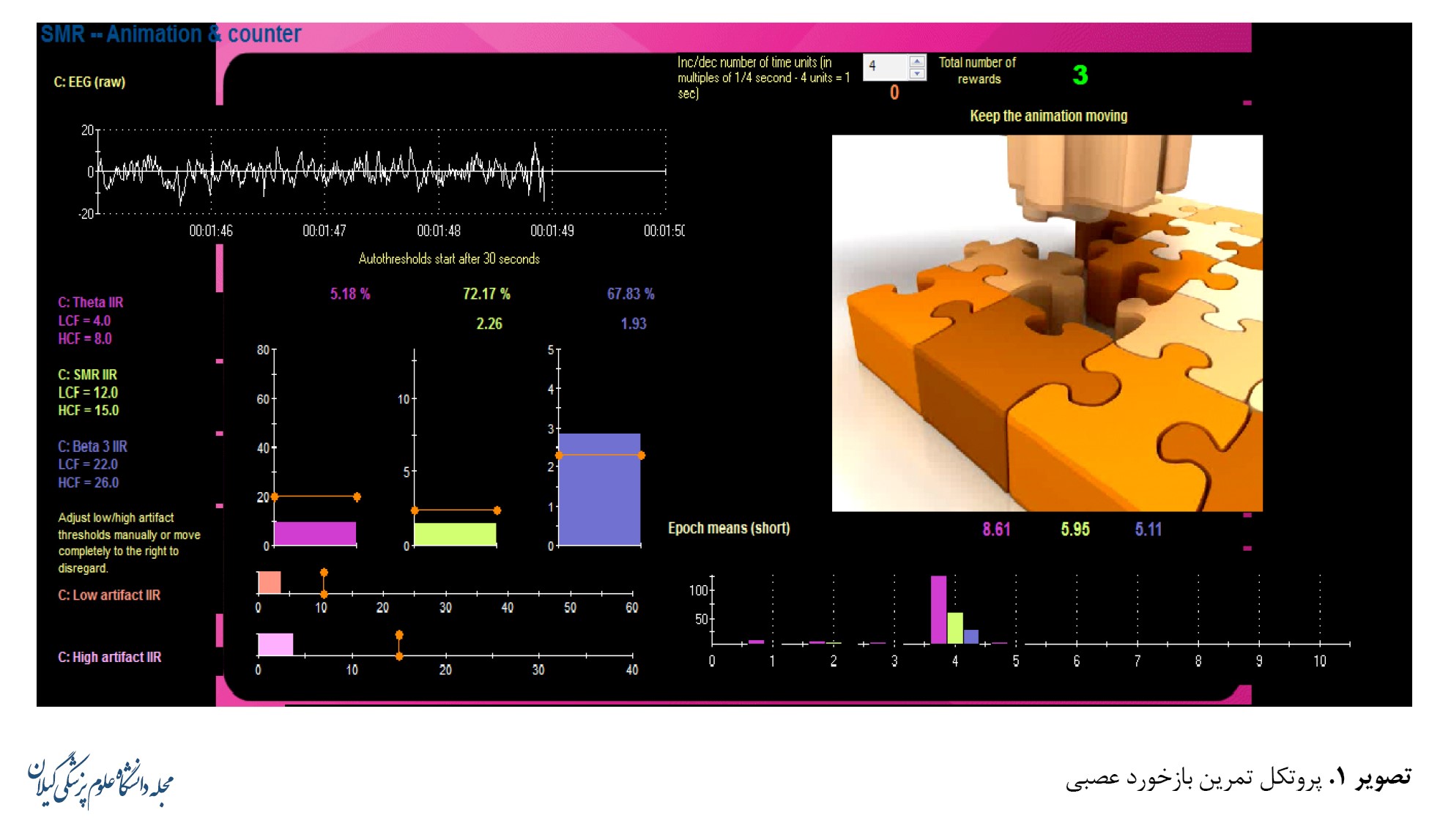
مداخله به مدت 8 هفته، 3 جلسه در هفته و هر جلسه 30 دقیقه انجام شد. پروتکل اجرایی براساس مطالعات پیشین انتخاب شد که شامل افزایش موج حسیحرکتی (12 تا 15 هرتز) و کاهش بتا (15 تا 20 هرتز) و تتا (4 تا 7 هرتز) در ناحیه CZ بود. براساس سیستم بینالمللی 10 تا 20 منطقه CZ مشخص شد. ناحیه CZ و لاله گوش با ژل لایهبردار مخصوص No-prep تمیز شدند. سپس یک الکترود فعال ازطریق چسب رسانای 10-20 در ناحیه CZ قرار داده شد. همچنین الکترودهای مرجع و گراند به ترتیب به گوش چپ و راست متصل شدند. «آستانه» آموزش توسط نرمافزار Biograph روی 80 درصد قرار گرفت. همچنین واحد زمان 0/5 ثانیه تنظیم شد. آستانه تمرین هر 4 جلسه براساس پیشرفت فردی کاهش مییابد و واحد زمان برای ارتقای سطح دشواری افزایش مییابد. روش اجرای مداخله بدین صورت بود که بیماران روبهروی مانیتور مینشستند و انیمیشنی برای آنان پخش میشد. زمانی که روند امواج حسیحرکتی، بتا وتتا برخلاف هدف مطالعه حاضر بود حرکت انیمیشن متوقف شده و زمانی که امواج مذکور در جهت مداخله حاضر تنظیم میشد انیمیشن حرکت میکرد. بیماران با حرکت انیمیشن و صدای خوشایند ناشی از امتیاز مثبت و هنگام توقف حرکت انیمیشن با صدای ناخوشایند ناشی از امتیاز منفی فیدبک بینایی و شنوایی لازم را برای تنظیم امواج مغزی خود دریافت میکردند (تصویر شماره 1).
کمردرد مزمن در سراسر جهان یکی از مهمترین مسائل پزشکی ازلحاظ کاهش کیفیت زندگی، ناتوانی و افزایش هزینههای اجتماعی و اقتصادی است [1]. بهطورکلی کمردرد در 2 دسته غیراختصاصی و مکانیکی طبقهبندی میشود. کمردرد مزمن غیراختصاصی 90 الی 95 درصد از کمردردها را شامل میشود و 20 درصد از جمعیت جهان را تحت تأثیر قرار میدهد [2 ,3]. کمردرد مزمن غیراختصاصی یک بیماری پیچیده و پاتوفیزیولوژی آن ناشناخته است که در مدت 3 ماه یا فراتر رخ میدهد [4]. شواهد قوی وجود دارد که نشان میدهد کمردرد با تعامل پیچیدهای از عوامل شناختی [5]، فیزیکی [6]، روانی [7]، نوروفیزیولوژیک [7] و سبک زندگی [8] مرتبط است. اگرچه بسیاری از این عوامل بهطور بالقوه قابلتغییر هستند، اغلب، پروتکلهای توانبخشی کمردرد مزمن بر مداخلات فیزیکی متمرکز است [9]. مداخلات فیزیکی ممکن است بر عوامل روانی تأثیری نداشته باشند [10].
عوامل روانشناختی نهتنها فعالیت قشر پردازش درد را تغییر میدهند، بلکه عملکرد مغز در قشر مربوط به توجه، پیشبینی و ناحیه احساسی درد را نیز تغییر میدهند [11]. مطالعات تغییرات قابلتوجهی را در مناطق کنترل درد، شناختی و سنسوری موتور، مانند تالاموس و قشر حسیحرکتی در زنان مبتلا به کمردرد مزمن گزارش کردند [12]. با تغییر نوروفیزیولوژیک سیستم عصبی مرکزی، یکپارچگی حسی مختل شده [13] و با افزایش توجه به محرکهای دردناک، کنترل حرکتی بیماران مبتلا به کمردرد مزمن تغییر میکند [14]. بنابراین لازم است مکانیسمهای عصبی که باعث درد، ناتوانی، اختلال حرکتی و اختلال در عملکرد سیستم عصبی مرکزی میشوند، شناسایی شوند [11]. در این راستا، مطالعات تصویربرداری عصبی، تغییرات ساختاری و عملکردی مغز را در شرایط درد مزمن اسکلتیعضلانی نشان داد. بهعنوان مثال محققان تغییراتی را در مورفولوژی و عملکرد مغز در بیماران مبتلا به کمردرد مزمن در مقایسه با گروه کنترل بدون درد گزارش کردند [15-17]. مطالعات پیشین با استفاده از تصویربرداری مغناطیسی، مگنتوآنسفالوگرافی، نوروفیدبک [15] و تحریک مغناطیسی ترانس کرانیال، بر روی بیماران مبتلا به کمردرد مزمن کاهش قابلتوجهی در تراکم ماده خاکستری در نواحی پیشپیشانی و تالاموس [18] و همچنین تغییرات در قشر حرکتی اولیه و سوماتوسنسوری [12] را نشان دادهاند.
اخیراً، تمرینات نوروفیدبک نیز مورد توجه محققان قرار گرفته است، زیرا اطلاعات قابلاعتمادی درمورد عملکرد مغز در حین استراحت، تحریک حسی و وظایف شناختی ارائه میدهد. علاوهبراین، این روش ایمن، ارزان و غیرتهاجمی است و آن را به یک دستگاه ارزشمند برای کاربردهای بالینی و تحقیقاتی تبدیل کرده است [19, 20]. علیرغم کاربرد گسترده نوروفیدبک برای ارزیابی تغییرات قشر مغز در شرایط درد مزمن اسکلتیعضلانی، دانش نسبتاً کمی درمورد تغییرات فعالیت امواج مغزی در بیماران کمردرد مزمن وجود دارد. نتایج مطالعه مرور سیستماتیک گزارش کرده است که تجربه درد با فعالیت امواج مغزی در ارتباط است. بدینصورت که در افراد مبتلا به دردهای مزمن مانند دردهای مزمن اعصاب کمری، امواج آلفا کاهش و امواج بتا و تتا افزایش پیدا میکند [21, 22]. بررسیهای سیستماتیک و متاآنالیزهای اخیر نشان میدهد تمرینات نوروفیدبک با هدف مدولاسیون شبکههای عصبی بدون هیچگونه تحریک الکتریکی بر مغز، مزایای بالینی معنیداری در کاهش شدت درد در افراد مبتلا به درد مزمن ارائه میدهد [23-25]. همچنین چارمز و همکاران در مطالعه خود بیان کردند بیماران مبتلا به درد مزمن که برای کنترل فعالیت نسبی قشر قدامی (ناحیه مرتبط با درمان و تجربه درد) تحت درمان نوروفیدبک بودند، کاهش درد پس از جلسات تمرینی را گزارش کردهاند [26]. اگرچه یافتههای اولیه امیدوارکننده است، اما تعداد اندکی مطالعه درمورد تأثیر مداخلاتی که فعالیت مغزی در افراد مبتلا به درد مزمن اسکلتیعضلانی را تغییر میدهد منتشر شده و سؤالات بسیاری در این زمینه وجود دارد که از رایجترین سؤالات سازوکار اثربخشی این نوع تمرینات در کاهش درد و نحوه طراحی پروتکلهای درمانی است. بنابراین هدف از مطالعه حاضر بررسی تأثیر نوروفیدبک بر متغیرهای روانشناختی در زنان مبتلا به کمردرد مزمن غیراختصاصی بود. براساس شواهد مذکور فرض کردیم تمرینات نوروفیدبک به کاهش درد، ناتوانی و ترس از حرکت منجر خواهد شد. امید است نتایج مطالعه بینشی جدید و کاربردی جهت درمان کمردرد مزمن غیراختصاصی فراهم کند.
روشها
پژوهش حاضر از نوع کارآزمایی بالینی و طرح پژوهشی پیشآزمون پسآزمون با گروه کنترل بود. جامعه آماری این پژوهش شامل زنان با کمردرد مزمن غیراختصاصی است که از کلینیکهای ارتوپدی یا پزشکی ورزشی استان همدان انتخاب شدند. از نرمافزار جیپاور نسخه 3/1/9/2 برای تخمین حجم نمونه استفاده شد. خروجی نرمافزار 30 نفر را گزارش کرد. با در نظر گرفتن ریزش 10 درصد برای 40 بیمار برنامهریزی شد. 40 نفر از بیماران مذکور بهصورت هدفمند انتخابشده و بهصورت تصادفی به 2 گروه آزمایش و کنترل (هر گروه 20 نفر) تقسیم شدند. معیارهای ورود: سابقه درد بیش از 12 هفته، نداشتن سابقه جراحی ستون فقرات و تعویض مفصل ران و دامنه سنی بین 30 الی 50 سال. معیارهای خروج: درد در سایر سگمنتال بدن، دفورمیتی شدید اندام تحتانی و فوقانی، سابقه جراحی، استفاده از داروهای ضددرد طی 6 ماه گذشته، فیزیوتراپی در 1 سال گذشته، شرکت در ورزش، درد سیاتیک، اسپاندیلولیز، اختلالات عصبیعضلانی، نورولوژیکی، تنفسی، اسپاسم عضلانی و شکستگی مهرهها. بیماران قبل از جمعآوری اطلاعات رضایتنامه آگاهانه را امضا کردند.
ارزیابیها
مقیاس بصری سنجش درد
درد با مقیاس آنالوگ بصری، 10 سانتیمتری ارزیابی شد. از بیمار خواسته شد که شدت درد را در طول فعالیتهای روزانه نشان دهد [27].
ناتوانی
شاخص ناتوانی اوسستوری برای ارزیابی ناتوانی استفاده شد (ICC=0/84) [28]. این شاخص 10 آیتم دارد و هر آیتم از 6 زیرمجموعه تشکیل شده است. درمجموع، میزان ناتوانی در 4 زیرمجموعه طبقهبندی میشود: امتیاز کمتر از 25 بهعنوان پایینترین سطح ناتوانی، امتیاز 25 الی50 بهعنوان ناتوانی متوسط، نمره 50 تا 75 بهعنوان ناتوانی شدید و نمره 75 تا 100 بهعنوان ناتوانی حاد [29].
کنزیوفوبیا
ترس از حرکت توسط مقیاس تامپا سنجیده شد. این پرسشنامه دارای 11 عبارت است. از آزمودنی خواسته شد تا هریک از عبارات را براساس احساس واقعی خود تکمیل کند و هدف آن ارزیابی میزان ترس از حرکت از ابعاد مختلف (باور به آسیبدیدگی، اجتناب از فعالیت) بود. طیف نمرهگذاری آن براساس طیف لیکرت 4 گزینهای ( به گزینه کاملاً مخالفم نمره 1 و به گزینه کاملاً موافقم نمره 4 تعلق میگیرد) بود [30].
مداخله نوروفیدبک
برای اجرای مداخله درمانی نوروفیدبک و ثبت بازخورد در این مطالعه، از دستگاه 8 کانالProcomp Infinity ساخت شرکت Toget Technology کانادا استفاده شد. این دستگاه دارای سختافزار Procomp و نرمافزار Biograph Infinity نسخه 5 است. لوازم جانبی دستگاه شامل سنسور امواج مغزی، سه الکترود: الکترود فعال(آبی)، الکترود مرجع (زرد)، الکترود زمین (مشکی)، تقویتکننده، واحد رابط TT-USB، کابل فیبر نوری و کابل USB بود.
مداخله به مدت 8 هفته، 3 جلسه در هفته و هر جلسه 30 دقیقه انجام شد. پروتکل اجرایی براساس مطالعات پیشین انتخاب شد که شامل افزایش موج حسیحرکتی (12 تا 15 هرتز) و کاهش بتا (15 تا 20 هرتز) و تتا (4 تا 7 هرتز) در ناحیه CZ بود. براساس سیستم بینالمللی 10 تا 20 منطقه CZ مشخص شد. ناحیه CZ و لاله گوش با ژل لایهبردار مخصوص No-prep تمیز شدند. سپس یک الکترود فعال ازطریق چسب رسانای 10-20 در ناحیه CZ قرار داده شد. همچنین الکترودهای مرجع و گراند به ترتیب به گوش چپ و راست متصل شدند. «آستانه» آموزش توسط نرمافزار Biograph روی 80 درصد قرار گرفت. همچنین واحد زمان 0/5 ثانیه تنظیم شد. آستانه تمرین هر 4 جلسه براساس پیشرفت فردی کاهش مییابد و واحد زمان برای ارتقای سطح دشواری افزایش مییابد. روش اجرای مداخله بدین صورت بود که بیماران روبهروی مانیتور مینشستند و انیمیشنی برای آنان پخش میشد. زمانی که روند امواج حسیحرکتی، بتا وتتا برخلاف هدف مطالعه حاضر بود حرکت انیمیشن متوقف شده و زمانی که امواج مذکور در جهت مداخله حاضر تنظیم میشد انیمیشن حرکت میکرد. بیماران با حرکت انیمیشن و صدای خوشایند ناشی از امتیاز مثبت و هنگام توقف حرکت انیمیشن با صدای ناخوشایند ناشی از امتیاز منفی فیدبک بینایی و شنوایی لازم را برای تنظیم امواج مغزی خود دریافت میکردند (تصویر شماره 1).
قبل از شروع جلسات اولیه و درمان، از بیماران خواسته شد مواردی را که ممکن است باعث ایجاد نویز شود، مانند انگشتر، تلفن همراه و ساعت را حذف کنند.
دادهها با استفاده از نرمافزار SPSS نسخه 26 مورد تجزیهوتحلیل قرار گرفت. در ابتدا آزمون شاپیروویلک برای اطمینان از توزیع نرمال دادهها استفاده شد. علاوهبراین، از آزمون لون بهمنظور بررسی همگنی واریانسها استفاده شد. درنتیجه، آزمون کوواریانس برای مقایسه نتایج بینگروهی استفاده شد و سطح معناداری 0/05 در نظر گرفته شد. اندازه اثر مداخلات ازطریق شاخص کوهن محاسبه شد. بهطورکلی، شاخص کوهن در سه دسته (0/01 اندازه اثر کوچک، 06/ اندازه اثر متوسط و 0/14 اندازه اثر بزرگ) طبقهبندی میشود.
یافتهها
مشخصات جمعیتشناختی گروهها در جدول شماره 1 خلاصه شده است.
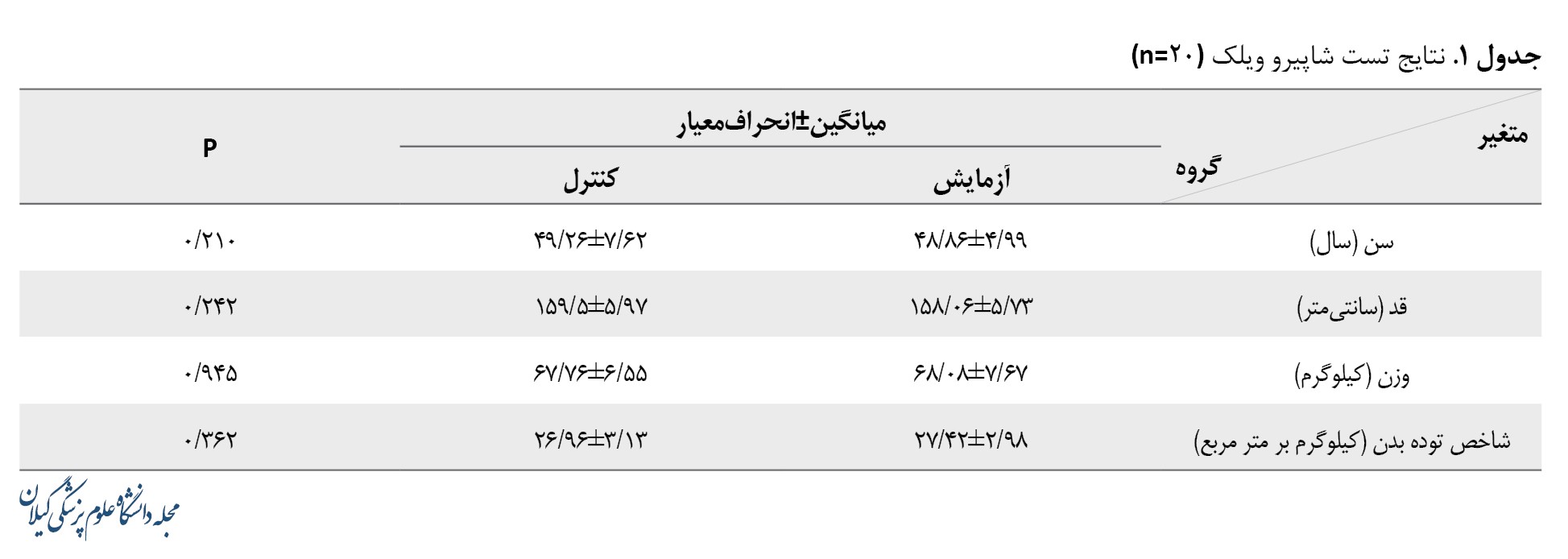
نتایج تست شاپیروویلک نشان داد توزیع دادهها نرمال است (0/050). نتایج آزمون کوواریانس در جدول شماره 2 ارائه شده است.
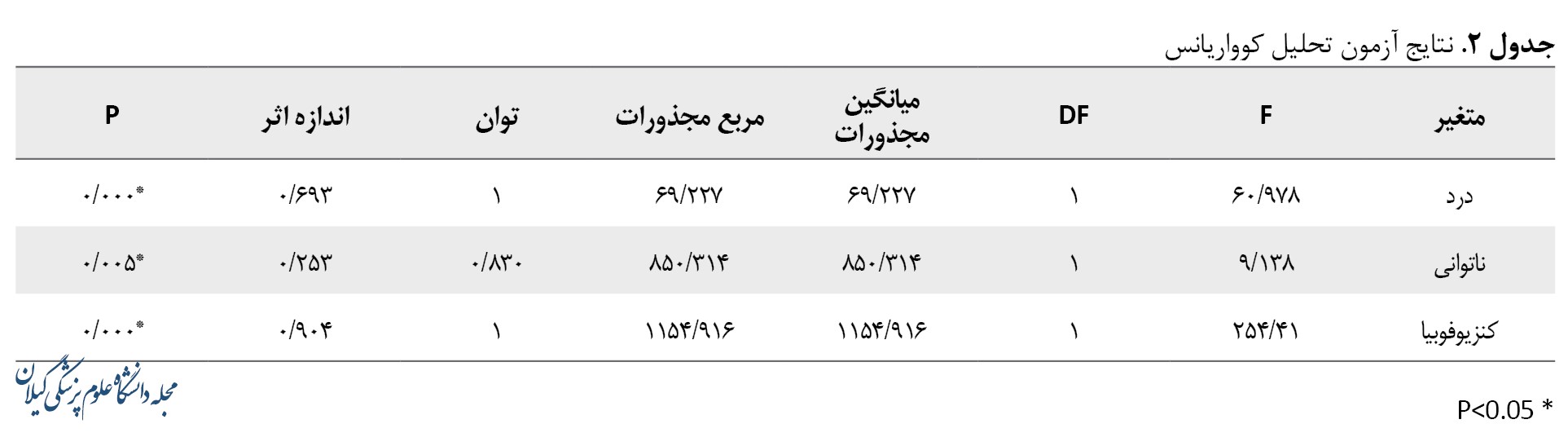
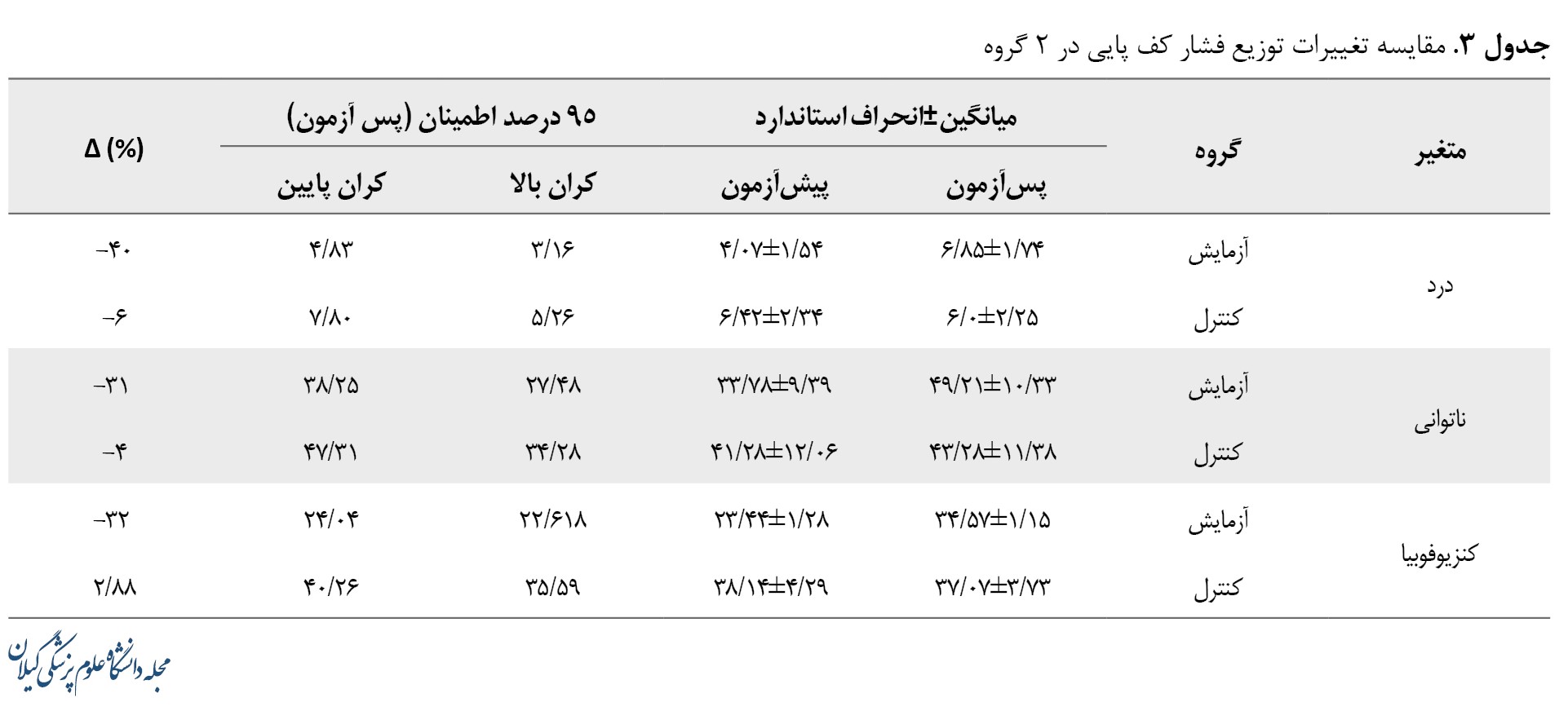
نتایج کوواریانس نشان داد تمرین نوروفیدبک با اندازه اثر بالا در کاهش درد (P=0/000 و 0/693=ƞ2)، ناتوانی (P=0/005 و ƞ2=0/253) و ترس از حرکت (P=0/000 و 0/904=ƞ2) تأثیر معناداری داشته است. در جدول شماره 3 آمار توصیفی نشان میدهد که گروه آزمایش یک کاهش 40 درصدی در کاهش درد، 31 درصدی در کاهش ناتوانی و 32 درصدی در کاهش ترس از حرکت داشته است.
بحث
هدف از این کارآزمایی تصادفی کنترلشده تأثیر تمرینات نوروفیدبک بر متغیرهای روانشناختی (درد، ناتوانی و ترس از حرکت) در زنان مبتلا به کمردرد مزمن غیراختصاصی بود. نتایج مطالعه حاضر بهبود قابلتوجهی را در شدت درد، ناتوانی و ترس از حرکت در بیماران موردمطالعه در مقایسه با پیشآزمون پس از 8 هفته مداخله تمرینات نوروفیدبک نشان داد.
نتایج مطالعه حاضر با مطالعات قبلی مطابقت دارد. بهعنوان مثال چارمز و همکاران در مطالعه خود بیان کردند بیماران مبتلا به درد مزمن که برای کنترل فعالیت نسبی قشر قدامی (ناحیه مرتبط با درمان و تجربه درد) تحت درمان نوروفیدبک بودند، کاهش درد پس از جلسات تمرینی را گزارش کردهاند [26]. همچنین مطالعه کایران و همکاران (2010) از اثربخشی نوروفیدبک بهعنوان درمانی برای بهبود درد و علائم روانی حمایت میکند [31]. مداخله در ناحیه CZ بهطور همزمان بر روی قشر حسیحرکتی، قشر حرکتی و سینگولیت تأثیر میگذارد [32]. به نظر می رسد تقویت امواج حسیحرکتی در قشر حسیحرکتی با سرکوب گیتهای آوران مرتبط باشد که منجر به مهار تالاموس، کاهش ایمپالسها و بیشفعالی میشود [31]. تالاموس دروازه ورود به قشر مغز است و تمام آورانهای حسیحرکتی از تالاموس میگذرد. افزایش فعالیت تالاموس با افزایش درک درد همراه است. درنتیجه منجر به افزایش ادراک آورانهای دردناک و تداوم علائم در طول زمان میشود [33]. به نظر میرسد تمرینات نوروفیدبک مکانیسمهای مهاری در تالاموس را تسهیل میکند و میتواند مسیرهای درد را بازیابی کند.
درد مزمن عملکرد قشر مغز را از مدار درد به احساسات تغییر میدهد. دیکفوس و همکاران (2019) گزارش کردند کنزیوفوبیا مربوط به فعالیت مغز در قشر حسیحرکتی، توجه و پردازش درد است [11]. قشر حسیحرکتی نقش مهمی در پردازش و ترس حافظه دارد. قشر حسیحرکتی به آمیگدال متصل است که نقش کلیدی در شناسایی و پردازش احساسات دارد. محرک درد باعث تغییر عصب انتقالدهنده آوران آمیگدال میشود. افزایش فعالیت آمیگدال در افراد مبتلا به ترس از حرکت ممکن است برای ارزیابی یا پاسخهای احتمالی به محرکهای دردناک پیشبینی شود. از طرفی افزایش توجه به حرکات دردناک ناشی از ترس، اضطراب و اجتناب را در افراد مبتلا به ترس از حرکت افزایش میدهد [34]. بنابراین به نظر میرسد در مطالعه حاضر بهبود فعالیت قشر حسیحرکتی و کاهش β که با اضطراب و توجه مرتبط است، منجر به اصلاح فعالیت غیر طبیعی آمیگدال و کاهش ترس و توجه شده است [35]. درنتیجه به نظر میرسد بخشی از درک درد و عوامل روانشناختی بیماران کمردرد مزمن غیراختصاصی تحت تأثیر تغییرات در پردازش سیستم عصبی مرکزی باشد. بهطورکلی، تمرینات نوروفیدبک بر امواج مغزی در پهنای باند خاصی تأثیر میگذارد که فرایندهای عصبی فیزیولوژیکی تجربه درد را منعکس میکند و آن را به حالت آرامش تغییر میدهد [36]. پاتریسیو و همکاران (2020) بیان کردند تحریک غیرتهاجمی مغز همراه با تمرینات کنترل حرکتی بر درد، ناتوانی و کنزیوفوبیا در افراد با کمردرد مزمن غیراختصاصی مؤثرتر از تمرین کنترل حرکتی بهتنهایی است [37].
استراتژیهایی مانند نوروفیدبک درزمینه مدولاسیون شبکههای عصبی، با مکانیسمهای بالقوهای مانند کاهش فعالیت امواج مغزی مرتبط با پردازش اطلاعات درد با کاهش مقاومت بیمار و تعامل فعال با درمان همراه است [17]. نتایج مطالعه مرور سیستماتیک نشان میدهد که درمان نوروفیدبک میتواند روند توان خوددرمانی مغز را افزایش داده و به بازگشت مجدد مغز به حالت اولیه خود برای عملکرد مطلوب کمک کند [17]. بنابراین در مطالعه حاضر بیماران در جلسات تمرین نوروفیدبک آموختند مناطق قشری و قسمت قدامی را که با پردازش و تجربه درد همراه است کنترل کنند و درنتیجه ترس و تجربه درد کاسته شد و به بهبودی عوامل روانشناختی درد منجر شد. باتوجه به عوامل مذکور به نظر میرسد شدت درد ادراکی در بیماران مبتلا به کمردرد مزمن واقعی نباشد و قسمت اعظم آن میتواند به عوامل روانشناختی درد مرتبط باشد [32].
نتیجهگیری
نتایج مطالعه حاضر نشان داد تمرینات نوروفیدبک بهعنوان یک مداخله درمانی غیرتهاجمی به کاهش شدت درد ادارکی منجر شد و سبب بهبودی ثانویه در موارد ترس از حرکت و ناتوانی شد. آموزش نوروفیدبک بهعنوان یکی از راهبردهای مؤثر در بهبود اختلالات روانی و جسمانی مختلف گسترش فراوانی یافته است. آموزش نوروفیدبک تکنیک شرطیسازی عاملی است که با استفاده از بازداری یا تقویت فعالیت امواج مغزی منجر به تغییر در عملکرد مغز شده و درنتیجه فرد را به اجرای مطلوب نزدیک میکند. درنتیجه توصیه میشود که متخصصین توانبخشی بهمنظور اثربخشی بهتر از ترکیب توأم مداخله درمانی نوروفیدبک و تمرینات فیزیکی استفاده کنند.
در این مطالعه ما 2 محدودیت داشتیم. اول، جامعه ما فقط زنان بودند. دوم، مهیا نبودن شرایط برای ارزیابی نتایج در بلندمدت. بنابراین توصیه میشود محققان تمرینات نوروفیدبک را در هر 2 جنس بیماران مبتلا به کمردرد مزمن غیراختصاصی و در بلندمدت ارزیابی کنند.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
این مطالعه در کمیته اخلاق دانشگاه بوعلی سینا همدان با (کد اخلاق IR.BASU.REC.1401.026) تصویب شد.
حامی مالی
این پژوهش هیچگونه کمک مالی از سازمانهای دولتی، خصوصی و غیرانتفاعی دریافت نکرده است.
مشارکت نویسندگان
مفهومسازی و طراحی مطالعه، تحلیل و تفسیر دادهها و ویرایش دستنوشته: علی یلفانی؛ تهیه پیشنویس دستنوشته، تحلیل آماری و جمعآوری دادهها: آزاده عسگرپور
تعارض منافع
بنابر اظهار نویسندگان، این مقاله تعارض منافع ندارد.
دادهها با استفاده از نرمافزار SPSS نسخه 26 مورد تجزیهوتحلیل قرار گرفت. در ابتدا آزمون شاپیروویلک برای اطمینان از توزیع نرمال دادهها استفاده شد. علاوهبراین، از آزمون لون بهمنظور بررسی همگنی واریانسها استفاده شد. درنتیجه، آزمون کوواریانس برای مقایسه نتایج بینگروهی استفاده شد و سطح معناداری 0/05 در نظر گرفته شد. اندازه اثر مداخلات ازطریق شاخص کوهن محاسبه شد. بهطورکلی، شاخص کوهن در سه دسته (0/01 اندازه اثر کوچک، 06/ اندازه اثر متوسط و 0/14 اندازه اثر بزرگ) طبقهبندی میشود.
یافتهها
مشخصات جمعیتشناختی گروهها در جدول شماره 1 خلاصه شده است.

نتایج تست شاپیروویلک نشان داد توزیع دادهها نرمال است (0/05

نتایج کوواریانس نشان داد تمرین نوروفیدبک با اندازه اثر بالا در کاهش درد (P=0/000 و 0/693=ƞ2)، ناتوانی (P=0/005 و ƞ2=0/253) و ترس از حرکت (P=0/000 و 0/904=ƞ2) تأثیر معناداری داشته است. در جدول شماره 3 آمار توصیفی نشان میدهد که گروه آزمایش یک کاهش 40 درصدی در کاهش درد، 31 درصدی در کاهش ناتوانی و 32 درصدی در کاهش ترس از حرکت داشته است.

بحث
هدف از این کارآزمایی تصادفی کنترلشده تأثیر تمرینات نوروفیدبک بر متغیرهای روانشناختی (درد، ناتوانی و ترس از حرکت) در زنان مبتلا به کمردرد مزمن غیراختصاصی بود. نتایج مطالعه حاضر بهبود قابلتوجهی را در شدت درد، ناتوانی و ترس از حرکت در بیماران موردمطالعه در مقایسه با پیشآزمون پس از 8 هفته مداخله تمرینات نوروفیدبک نشان داد.
نتایج مطالعه حاضر با مطالعات قبلی مطابقت دارد. بهعنوان مثال چارمز و همکاران در مطالعه خود بیان کردند بیماران مبتلا به درد مزمن که برای کنترل فعالیت نسبی قشر قدامی (ناحیه مرتبط با درمان و تجربه درد) تحت درمان نوروفیدبک بودند، کاهش درد پس از جلسات تمرینی را گزارش کردهاند [26]. همچنین مطالعه کایران و همکاران (2010) از اثربخشی نوروفیدبک بهعنوان درمانی برای بهبود درد و علائم روانی حمایت میکند [31]. مداخله در ناحیه CZ بهطور همزمان بر روی قشر حسیحرکتی، قشر حرکتی و سینگولیت تأثیر میگذارد [32]. به نظر می رسد تقویت امواج حسیحرکتی در قشر حسیحرکتی با سرکوب گیتهای آوران مرتبط باشد که منجر به مهار تالاموس، کاهش ایمپالسها و بیشفعالی میشود [31]. تالاموس دروازه ورود به قشر مغز است و تمام آورانهای حسیحرکتی از تالاموس میگذرد. افزایش فعالیت تالاموس با افزایش درک درد همراه است. درنتیجه منجر به افزایش ادراک آورانهای دردناک و تداوم علائم در طول زمان میشود [33]. به نظر میرسد تمرینات نوروفیدبک مکانیسمهای مهاری در تالاموس را تسهیل میکند و میتواند مسیرهای درد را بازیابی کند.
درد مزمن عملکرد قشر مغز را از مدار درد به احساسات تغییر میدهد. دیکفوس و همکاران (2019) گزارش کردند کنزیوفوبیا مربوط به فعالیت مغز در قشر حسیحرکتی، توجه و پردازش درد است [11]. قشر حسیحرکتی نقش مهمی در پردازش و ترس حافظه دارد. قشر حسیحرکتی به آمیگدال متصل است که نقش کلیدی در شناسایی و پردازش احساسات دارد. محرک درد باعث تغییر عصب انتقالدهنده آوران آمیگدال میشود. افزایش فعالیت آمیگدال در افراد مبتلا به ترس از حرکت ممکن است برای ارزیابی یا پاسخهای احتمالی به محرکهای دردناک پیشبینی شود. از طرفی افزایش توجه به حرکات دردناک ناشی از ترس، اضطراب و اجتناب را در افراد مبتلا به ترس از حرکت افزایش میدهد [34]. بنابراین به نظر میرسد در مطالعه حاضر بهبود فعالیت قشر حسیحرکتی و کاهش β که با اضطراب و توجه مرتبط است، منجر به اصلاح فعالیت غیر طبیعی آمیگدال و کاهش ترس و توجه شده است [35]. درنتیجه به نظر میرسد بخشی از درک درد و عوامل روانشناختی بیماران کمردرد مزمن غیراختصاصی تحت تأثیر تغییرات در پردازش سیستم عصبی مرکزی باشد. بهطورکلی، تمرینات نوروفیدبک بر امواج مغزی در پهنای باند خاصی تأثیر میگذارد که فرایندهای عصبی فیزیولوژیکی تجربه درد را منعکس میکند و آن را به حالت آرامش تغییر میدهد [36]. پاتریسیو و همکاران (2020) بیان کردند تحریک غیرتهاجمی مغز همراه با تمرینات کنترل حرکتی بر درد، ناتوانی و کنزیوفوبیا در افراد با کمردرد مزمن غیراختصاصی مؤثرتر از تمرین کنترل حرکتی بهتنهایی است [37].
استراتژیهایی مانند نوروفیدبک درزمینه مدولاسیون شبکههای عصبی، با مکانیسمهای بالقوهای مانند کاهش فعالیت امواج مغزی مرتبط با پردازش اطلاعات درد با کاهش مقاومت بیمار و تعامل فعال با درمان همراه است [17]. نتایج مطالعه مرور سیستماتیک نشان میدهد که درمان نوروفیدبک میتواند روند توان خوددرمانی مغز را افزایش داده و به بازگشت مجدد مغز به حالت اولیه خود برای عملکرد مطلوب کمک کند [17]. بنابراین در مطالعه حاضر بیماران در جلسات تمرین نوروفیدبک آموختند مناطق قشری و قسمت قدامی را که با پردازش و تجربه درد همراه است کنترل کنند و درنتیجه ترس و تجربه درد کاسته شد و به بهبودی عوامل روانشناختی درد منجر شد. باتوجه به عوامل مذکور به نظر میرسد شدت درد ادراکی در بیماران مبتلا به کمردرد مزمن واقعی نباشد و قسمت اعظم آن میتواند به عوامل روانشناختی درد مرتبط باشد [32].
نتیجهگیری
نتایج مطالعه حاضر نشان داد تمرینات نوروفیدبک بهعنوان یک مداخله درمانی غیرتهاجمی به کاهش شدت درد ادارکی منجر شد و سبب بهبودی ثانویه در موارد ترس از حرکت و ناتوانی شد. آموزش نوروفیدبک بهعنوان یکی از راهبردهای مؤثر در بهبود اختلالات روانی و جسمانی مختلف گسترش فراوانی یافته است. آموزش نوروفیدبک تکنیک شرطیسازی عاملی است که با استفاده از بازداری یا تقویت فعالیت امواج مغزی منجر به تغییر در عملکرد مغز شده و درنتیجه فرد را به اجرای مطلوب نزدیک میکند. درنتیجه توصیه میشود که متخصصین توانبخشی بهمنظور اثربخشی بهتر از ترکیب توأم مداخله درمانی نوروفیدبک و تمرینات فیزیکی استفاده کنند.
در این مطالعه ما 2 محدودیت داشتیم. اول، جامعه ما فقط زنان بودند. دوم، مهیا نبودن شرایط برای ارزیابی نتایج در بلندمدت. بنابراین توصیه میشود محققان تمرینات نوروفیدبک را در هر 2 جنس بیماران مبتلا به کمردرد مزمن غیراختصاصی و در بلندمدت ارزیابی کنند.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
این مطالعه در کمیته اخلاق دانشگاه بوعلی سینا همدان با (کد اخلاق IR.BASU.REC.1401.026) تصویب شد.
حامی مالی
این پژوهش هیچگونه کمک مالی از سازمانهای دولتی، خصوصی و غیرانتفاعی دریافت نکرده است.
مشارکت نویسندگان
مفهومسازی و طراحی مطالعه، تحلیل و تفسیر دادهها و ویرایش دستنوشته: علی یلفانی؛ تهیه پیشنویس دستنوشته، تحلیل آماری و جمعآوری دادهها: آزاده عسگرپور
تعارض منافع
بنابر اظهار نویسندگان، این مقاله تعارض منافع ندارد.
References
1.Phattharasupharerk S, Purepong N, Eksakulkla S, Siriphorn A. Effects of Qigong practice in office workers with chronic non-specific low back pain: A randomized control trial. Journal of Bodywork and Movement Therapies. 2019; 23(2):375-81. [DOI:10.1016/j.jbmt.2018.02.004] [PMID]
2.Goossens N, Janssens L, Caeyenberghs K, Albouy G, Brumagne S. Differences in brain processing of proprioception related to postural control in patients with recurrent non-specific low back pain and healthy controls. NeuroImage Clinical. 2019; 23:101881. [DOI:10.1016/j.nicl.2019.101881] [PMID]
3.Verbrugghe J, Agten A, Stevens S, Vandenabeele F, Roussel N, Verbunt J, et al. High intensity training improves symptoms of central sensitization at six-month follow-up in persons with chronic nonspecific low back pain: Secondary analysis of a randomized controlled trial. Brazilian Journal of Physical Therapy. 2023; 27(2):100496. [DOI:10.1016/j.bjpt.2023.100496] [PMID]
4.Turci AM, Nogueira CG, Nogueira Carrer HC, Chaves TC. Self-administered stretching exercises are as effective as motor control exercises for people with chronic non-specific low back pain: A randomised trial. Journal of Physiotherapy. 2023; 69 (2):93-9. [DOI:10.1016/j.jphys.2023.02.016] [PMID]
5.Campbell P, Bishop A, Dunn KM, Main CJ, Thomas E, Foster NE. Conceptual overlap of psychological constructs in low back pain. Pain. 2013; 54(9):1783-91. [DOI:10.1016/j.pain.2013.05.035] [PMID]
6.Dankaerts W, O'Sullivan P, Burnett A, Straker L, Davey P, Gupta R. Discriminating healthy controls and two clinical subgroups of nonspecific chronic low back pain patients using trunk muscle activation and lumbosacral kinematics of postures and movements: A statistical classification model. Spine. 2009; 34(15):1610-8. [DOI:10.1097/BRS.0b013e3181aa6175] [PMID]
7.Lee H, Hübscher M, Moseley GL, Kamper SJ, Traeger AC, Mansell G, et al. How does pain lead to disability? A systematic review and meta-analysis of mediation studies in people with back and neck pain. Pain. 2015; 156(6):988-97. [DOI:10.1097/j.pain.0000000000000146] [PMID]
8.Briggs AM, Jordan JE, O'Sullivan PB, Buchbinder R, Burnett AF, Osborne RH, et al. Individuals with chronic low back pain have greater di¨culty in engaging in positive lifestyle behaviours than those without back pain: An assessment of health literacy. BMC Musculoskeletal Disorders. 2011; 12:161. [DOI:10.1186/1471-2474-12-161] [PMID]
9.Lack S, Neal B, De Oliveira Silva D, Barton C. How to manage patellofemoral pain-Understanding the multifactorial nature and treatment options. Physical Therapy in Sport. 2018; 32:155-66. [PMID]
10.Selhorst M, Hoehn J, Degenhart T, Schmitt L, Fernandez-Fernandez A. Psychologically- informed video reduces maladaptive beliefs in adolescents with patellofemoral pain. Physical Therapy in Sport. 2020; 41:23-8. [DOI:10.1016/j.ptsp.2019.10.009] [PMID]
11.Diekfuss JA, Saltman AJ, Grooms DR, Bonnette S, Foss KB, Berz K, et al. Neural correlates of knee motor control for young females with patellofemoral pain. Orthopaedic Journal of Sports Medicine. 2019; 7 (3_suppl):2325967119S0001. [DOI:10.1177/2325967119S00012]
12.Kregel J, Meeus M, Malfliet A, Dolphens M, Danneels L, Nijs J, et al. Structural and functional brain abnormalities in chronic low back pain: A systematic review. Seminars in Arthritis and Rheumatism. 2015; 45(2):229-37. [DOI:10.1016/j.semarthrit.2015.05.002] [PMID]
13.Diekfuss JA, Grooms DR, Coghill RC, Nissen KS, Saltman AJ, Berz K, et al. Kinesiophobia is related to brain activity for knee motor control in pediatric patients with patellofemoral pain. Orthopaedic Journal of Sports Medicine. 2020; 8(4_suppl3):2325967120S00187. [DOI:10.1177/2325967120S00187]
14.Li Y, Xu Z, Xie H, Fu R, Lo WLA, Cheng X, et al. Changes in cortical activation during upright stance in individuals with chronic low back pain: An fNIRS study. Frontiers in Human Neuroscience. 2023; 17:1085831. [DOI:10.3389/fnhum.2023.1085831] [PMID]
15.Apkarian AV, Sosa Y, Sonty S, Levy RM, Harden RN, Parrish TB, et al. Chronic back pain is associated with decreased prefrontal and thalamic gray matter density. Journal of Neuroscience. 2004; 24(46):10410-5. [DOI:10.1523/JNEUROSCI.2541-04.2004] [PMID]
16.Giesecke T, Gracely RH, Grant MA, Nachemson A, Petzke F, Williams DA, et al. Evidence of augmented central pain processing in idiopathic chronic low back pain. Arthritis and Rheumatism. 2004; 50(2):613-23. [DOI:10.1002/art.20063] [PMID]
17.Schouppe S, Van Oosterwijck S, Danneels L, Van Damme S, & Van Oosterwijck J. Are functional brain alterations present in low back pain? A systematic review of EEG studies. The Journal of Pain. 2020; 21(1-2):25-43. [DOI:10.1016/j.jpain.2019.06.010] [PMID]
18.Gracely RH, Geisser ME, Giesecke T, Grant MA, Petzke F, Williams DA, et al. Pain catastrophizing and neural responses to pain among persons with fibromyalgia. Brain. 2004; 127(4):835-43. [DOI:10.1093/brain/awh098] [PMID]
19.de Vries M, Wilder-Smith OH, Jongsma ML, van den Broeke EN, Arns M, van Goor H, et al. Altered resting state EEG in chronic pancreatitis patients: Toward a marker for chronic pain. Journal of Pain Research. 2013; 6:815-24. [DOI:10.2147/JPR.S50919] [PMID]
20.Spronk D, Arns M, Barnett KJ, Cooper NJ, Gordon E. An investigation of EEG, genetic and cognitive markers of treatment response to antidepressant medication in patients with major depressive disorder: A pilot study. Journal of Affective Disorders. 2011; 128(1-2):41-8. [DOI:10.1016/j.jad.2010.06.021] [PMID]
21.Miró J, Castarlenas E, de la Vega R, Roy R, Solé E, Tomé-Pires C, et al. Psychological neuromodulatory treatments for young people with chronic pain. Children. 2016; 3(4):41. [DOI:10.3390/children3040041] [PMID]
22.Ibric VL. Neurofeedback training enhanced by light and/or electromagnetic closed-loop EEG induces analgesia in patients with neuropathic pain syndromes. Pain. 2002; 11:439-40. [Link]
23.Patel K, Sutherland H, Henshaw J, Taylor JR, Brown CA, Casson AJ, et al. Effects of neurofeedback in the management of chronic pain: A systematic review and metaanalysis of clinical trials. European Journal of Pain. 2020; 24(8):1440-57.[DOI:10.1002/ejp.1612] [PMID]
24.Roy R, de la Vega R, Jensen MP, Miró J. Neurofeedback for pain management: A systematic review. Frontiers in Neuroscience. 2020; 14:671. [DOI:10.3389/fnins.2020.00671] [PMID]
25.Hesam-Shariati N, Chang WJ, Wewege MA, McAuley JH, Booth A, Trost Z, et al. The analgesic effect of electroencephalographic neurofeedback for people with chronic pain: A systematic review and metaanalysis. European Journal of Neurology. 2022; 29(3):921-36. [DOI:10.1111/ene.15189] [PMID]
26.deCharms RC, Maeda F, Glover GH, Ludlow D, Pauly JM, Soneji D, et al. Control over brain activation and pain learned by using real-time functional MRI. Proceedings of the National Academy of Sciences of the United States of America. 2005; 102(51):18626-31. [DOI:10.1073/pnas.0505210102] [PMID]
27.Armstrong K, Gokal R, Chevalier A, Todorsky W, Lim M. Microcurrent point stimulation applied to lower back acupuncture points for the treatment of nonspecific neck pain. Journal of Alternative and Complementary Medicine. 2017; 23(4):295-9. [DOI:10.1089/acm.2016.0313] [PMID]
28.Inani SB, Selkar SP. Effect of core stabilization exercises versus conventional exercises on pain and functional status in patients with non-specific low back pain: A randomized clinical trial. Journal of Back and Musculoskeletal Rehabilitation. 2013; 26(1):37-43. [DOI:10.3233/BMR-2012-0348] [PMID]
29.Yalfani A, Raeisi Z, Koumasian Z. Effects of eight-week water versus mat Pilates on female patients with chronic nonspecific low back pain: Double-blind randomized clinical trial. Journal of Bodywork and Movement Therapies. 2020; 24(4):70-5. [DOI:10.1016/j.jbmt.2020.06.002] [PMID]
30.da Silva RA, Vieira ER, Carvalho CE, Oliveira MR, Amorim CF, Neto EN. Age-related differences on low back pain and postural control during one-leg stance: A case-control study. European Spine Journal. 2016; 25(4):1251-7. [DOI:10.1007/s00586-015-4255-9] [PMID]
31.Kayıran S, Dursun E, Dursun N, Ermutlu N, Karamürsel S. Neurofeedback intervention in fibromyalgia syndrome; A randomized, controlled, rater blind clinical trial. Journal of Applied Psychophysiology and Biofeedback. 2010; 35(4):293-302. [DOI:10.1007/s10484-010-9135-9] [PMID]
32.Ahmadi M, Yalfani A, Gandomi F, Rashid K. [The effect of twelve week neurofeedback training on perceptual pain, intensity, fear of pain, pelvic drop, and dynamic knee valgus index in men with patellofemoral pain syndrome: A randomized double blind clinical trial (Persian)]. Sadra Medical Journal. 2020; 8(2):151-64. [Link]
33.Bismuth J, Vialatte F, Lefaucheur JP. Relieving peripheral neuropathic pain by increasing the power-ratio of low-β over high-β activities in the central cortical region with EEG-based neurofeedback: Study protocol for a controlled pilot trial (SMRPain study). Clinical Neurophysiology. 2020; 50(1):5-20. [PMID]
34.Meier ML, Stämpfli P, Vrana A, Humphreys BK, Seifritz E, Hotz-Boendermaker S. Neural correlates of fear of movement in patients with chronic low back pain vs. pain-free individuals. Frontiers in Human Neuroscience. 2016; 10:386. [DOI:10.3389/fnhum.2016.00386]
35.Terrasa JL, Barros-Loscertales A, Montoya P, Muñoz MA. Self-regulation of SMR power led to an enhancement of functional connectivity of somatomotor cortices in fibromyalgia patients. Frontiers in Neuroscience. 2020; 14:236. [DOI:10.3389/fnins.2020.00236] [PMID]
36.Jensen MP, Day MA, Miró J. Neuromodulatory treatments for chronic pain: Efficacy and mechanisms. Nature Reviews. Neurology. 2014; 10(3):167-78. [DOI:10.1038/nrneurol.2014.12] [PMID]
37.Patricio P, Roy JS, Macedo L, Roy M, Léonard G, Hodges P, et al. Repetitive transcranial magnetic stimulation alone and in combination with motor control exercise for the treatment of individuals with chronic non-specific low back pain (ExTraStim trial): Study protocol for a randomised controlled trial. BMJ Open. 2021; 11(3):e045504. [DOI:10.1136/bmjopen-2020-045504] [PMID]
1.Phattharasupharerk S, Purepong N, Eksakulkla S, Siriphorn A. Effects of Qigong practice in office workers with chronic non-specific low back pain: A randomized control trial. Journal of Bodywork and Movement Therapies. 2019; 23(2):375-81. [DOI:10.1016/j.jbmt.2018.02.004] [PMID]
2.Goossens N, Janssens L, Caeyenberghs K, Albouy G, Brumagne S. Differences in brain processing of proprioception related to postural control in patients with recurrent non-specific low back pain and healthy controls. NeuroImage Clinical. 2019; 23:101881. [DOI:10.1016/j.nicl.2019.101881] [PMID]
3.Verbrugghe J, Agten A, Stevens S, Vandenabeele F, Roussel N, Verbunt J, et al. High intensity training improves symptoms of central sensitization at six-month follow-up in persons with chronic nonspecific low back pain: Secondary analysis of a randomized controlled trial. Brazilian Journal of Physical Therapy. 2023; 27(2):100496. [DOI:10.1016/j.bjpt.2023.100496] [PMID]
4.Turci AM, Nogueira CG, Nogueira Carrer HC, Chaves TC. Self-administered stretching exercises are as effective as motor control exercises for people with chronic non-specific low back pain: A randomised trial. Journal of Physiotherapy. 2023; 69 (2):93-9. [DOI:10.1016/j.jphys.2023.02.016] [PMID]
5.Campbell P, Bishop A, Dunn KM, Main CJ, Thomas E, Foster NE. Conceptual overlap of psychological constructs in low back pain. Pain. 2013; 54(9):1783-91. [DOI:10.1016/j.pain.2013.05.035] [PMID]
6.Dankaerts W, O'Sullivan P, Burnett A, Straker L, Davey P, Gupta R. Discriminating healthy controls and two clinical subgroups of nonspecific chronic low back pain patients using trunk muscle activation and lumbosacral kinematics of postures and movements: A statistical classification model. Spine. 2009; 34(15):1610-8. [DOI:10.1097/BRS.0b013e3181aa6175] [PMID]
7.Lee H, Hübscher M, Moseley GL, Kamper SJ, Traeger AC, Mansell G, et al. How does pain lead to disability? A systematic review and meta-analysis of mediation studies in people with back and neck pain. Pain. 2015; 156(6):988-97. [DOI:10.1097/j.pain.0000000000000146] [PMID]
8.Briggs AM, Jordan JE, O'Sullivan PB, Buchbinder R, Burnett AF, Osborne RH, et al. Individuals with chronic low back pain have greater di¨culty in engaging in positive lifestyle behaviours than those without back pain: An assessment of health literacy. BMC Musculoskeletal Disorders. 2011; 12:161. [DOI:10.1186/1471-2474-12-161] [PMID]
9.Lack S, Neal B, De Oliveira Silva D, Barton C. How to manage patellofemoral pain-Understanding the multifactorial nature and treatment options. Physical Therapy in Sport. 2018; 32:155-66. [PMID]
10.Selhorst M, Hoehn J, Degenhart T, Schmitt L, Fernandez-Fernandez A. Psychologically- informed video reduces maladaptive beliefs in adolescents with patellofemoral pain. Physical Therapy in Sport. 2020; 41:23-8. [DOI:10.1016/j.ptsp.2019.10.009] [PMID]
11.Diekfuss JA, Saltman AJ, Grooms DR, Bonnette S, Foss KB, Berz K, et al. Neural correlates of knee motor control for young females with patellofemoral pain. Orthopaedic Journal of Sports Medicine. 2019; 7 (3_suppl):2325967119S0001. [DOI:10.1177/2325967119S00012]
12.Kregel J, Meeus M, Malfliet A, Dolphens M, Danneels L, Nijs J, et al. Structural and functional brain abnormalities in chronic low back pain: A systematic review. Seminars in Arthritis and Rheumatism. 2015; 45(2):229-37. [DOI:10.1016/j.semarthrit.2015.05.002] [PMID]
13.Diekfuss JA, Grooms DR, Coghill RC, Nissen KS, Saltman AJ, Berz K, et al. Kinesiophobia is related to brain activity for knee motor control in pediatric patients with patellofemoral pain. Orthopaedic Journal of Sports Medicine. 2020; 8(4_suppl3):2325967120S00187. [DOI:10.1177/2325967120S00187]
14.Li Y, Xu Z, Xie H, Fu R, Lo WLA, Cheng X, et al. Changes in cortical activation during upright stance in individuals with chronic low back pain: An fNIRS study. Frontiers in Human Neuroscience. 2023; 17:1085831. [DOI:10.3389/fnhum.2023.1085831] [PMID]
15.Apkarian AV, Sosa Y, Sonty S, Levy RM, Harden RN, Parrish TB, et al. Chronic back pain is associated with decreased prefrontal and thalamic gray matter density. Journal of Neuroscience. 2004; 24(46):10410-5. [DOI:10.1523/JNEUROSCI.2541-04.2004] [PMID]
16.Giesecke T, Gracely RH, Grant MA, Nachemson A, Petzke F, Williams DA, et al. Evidence of augmented central pain processing in idiopathic chronic low back pain. Arthritis and Rheumatism. 2004; 50(2):613-23. [DOI:10.1002/art.20063] [PMID]
17.Schouppe S, Van Oosterwijck S, Danneels L, Van Damme S, & Van Oosterwijck J. Are functional brain alterations present in low back pain? A systematic review of EEG studies. The Journal of Pain. 2020; 21(1-2):25-43. [DOI:10.1016/j.jpain.2019.06.010] [PMID]
18.Gracely RH, Geisser ME, Giesecke T, Grant MA, Petzke F, Williams DA, et al. Pain catastrophizing and neural responses to pain among persons with fibromyalgia. Brain. 2004; 127(4):835-43. [DOI:10.1093/brain/awh098] [PMID]
19.de Vries M, Wilder-Smith OH, Jongsma ML, van den Broeke EN, Arns M, van Goor H, et al. Altered resting state EEG in chronic pancreatitis patients: Toward a marker for chronic pain. Journal of Pain Research. 2013; 6:815-24. [DOI:10.2147/JPR.S50919] [PMID]
20.Spronk D, Arns M, Barnett KJ, Cooper NJ, Gordon E. An investigation of EEG, genetic and cognitive markers of treatment response to antidepressant medication in patients with major depressive disorder: A pilot study. Journal of Affective Disorders. 2011; 128(1-2):41-8. [DOI:10.1016/j.jad.2010.06.021] [PMID]
21.Miró J, Castarlenas E, de la Vega R, Roy R, Solé E, Tomé-Pires C, et al. Psychological neuromodulatory treatments for young people with chronic pain. Children. 2016; 3(4):41. [DOI:10.3390/children3040041] [PMID]
22.Ibric VL. Neurofeedback training enhanced by light and/or electromagnetic closed-loop EEG induces analgesia in patients with neuropathic pain syndromes. Pain. 2002; 11:439-40. [Link]
23.Patel K, Sutherland H, Henshaw J, Taylor JR, Brown CA, Casson AJ, et al. Effects of neurofeedback in the management of chronic pain: A systematic review and metaanalysis of clinical trials. European Journal of Pain. 2020; 24(8):1440-57.[DOI:10.1002/ejp.1612] [PMID]
24.Roy R, de la Vega R, Jensen MP, Miró J. Neurofeedback for pain management: A systematic review. Frontiers in Neuroscience. 2020; 14:671. [DOI:10.3389/fnins.2020.00671] [PMID]
25.Hesam-Shariati N, Chang WJ, Wewege MA, McAuley JH, Booth A, Trost Z, et al. The analgesic effect of electroencephalographic neurofeedback for people with chronic pain: A systematic review and metaanalysis. European Journal of Neurology. 2022; 29(3):921-36. [DOI:10.1111/ene.15189] [PMID]
26.deCharms RC, Maeda F, Glover GH, Ludlow D, Pauly JM, Soneji D, et al. Control over brain activation and pain learned by using real-time functional MRI. Proceedings of the National Academy of Sciences of the United States of America. 2005; 102(51):18626-31. [DOI:10.1073/pnas.0505210102] [PMID]
27.Armstrong K, Gokal R, Chevalier A, Todorsky W, Lim M. Microcurrent point stimulation applied to lower back acupuncture points for the treatment of nonspecific neck pain. Journal of Alternative and Complementary Medicine. 2017; 23(4):295-9. [DOI:10.1089/acm.2016.0313] [PMID]
28.Inani SB, Selkar SP. Effect of core stabilization exercises versus conventional exercises on pain and functional status in patients with non-specific low back pain: A randomized clinical trial. Journal of Back and Musculoskeletal Rehabilitation. 2013; 26(1):37-43. [DOI:10.3233/BMR-2012-0348] [PMID]
29.Yalfani A, Raeisi Z, Koumasian Z. Effects of eight-week water versus mat Pilates on female patients with chronic nonspecific low back pain: Double-blind randomized clinical trial. Journal of Bodywork and Movement Therapies. 2020; 24(4):70-5. [DOI:10.1016/j.jbmt.2020.06.002] [PMID]
30.da Silva RA, Vieira ER, Carvalho CE, Oliveira MR, Amorim CF, Neto EN. Age-related differences on low back pain and postural control during one-leg stance: A case-control study. European Spine Journal. 2016; 25(4):1251-7. [DOI:10.1007/s00586-015-4255-9] [PMID]
31.Kayıran S, Dursun E, Dursun N, Ermutlu N, Karamürsel S. Neurofeedback intervention in fibromyalgia syndrome; A randomized, controlled, rater blind clinical trial. Journal of Applied Psychophysiology and Biofeedback. 2010; 35(4):293-302. [DOI:10.1007/s10484-010-9135-9] [PMID]
32.Ahmadi M, Yalfani A, Gandomi F, Rashid K. [The effect of twelve week neurofeedback training on perceptual pain, intensity, fear of pain, pelvic drop, and dynamic knee valgus index in men with patellofemoral pain syndrome: A randomized double blind clinical trial (Persian)]. Sadra Medical Journal. 2020; 8(2):151-64. [Link]
33.Bismuth J, Vialatte F, Lefaucheur JP. Relieving peripheral neuropathic pain by increasing the power-ratio of low-β over high-β activities in the central cortical region with EEG-based neurofeedback: Study protocol for a controlled pilot trial (SMRPain study). Clinical Neurophysiology. 2020; 50(1):5-20. [PMID]
34.Meier ML, Stämpfli P, Vrana A, Humphreys BK, Seifritz E, Hotz-Boendermaker S. Neural correlates of fear of movement in patients with chronic low back pain vs. pain-free individuals. Frontiers in Human Neuroscience. 2016; 10:386. [DOI:10.3389/fnhum.2016.00386]
35.Terrasa JL, Barros-Loscertales A, Montoya P, Muñoz MA. Self-regulation of SMR power led to an enhancement of functional connectivity of somatomotor cortices in fibromyalgia patients. Frontiers in Neuroscience. 2020; 14:236. [DOI:10.3389/fnins.2020.00236] [PMID]
36.Jensen MP, Day MA, Miró J. Neuromodulatory treatments for chronic pain: Efficacy and mechanisms. Nature Reviews. Neurology. 2014; 10(3):167-78. [DOI:10.1038/nrneurol.2014.12] [PMID]
37.Patricio P, Roy JS, Macedo L, Roy M, Léonard G, Hodges P, et al. Repetitive transcranial magnetic stimulation alone and in combination with motor control exercise for the treatment of individuals with chronic non-specific low back pain (ExTraStim trial): Study protocol for a randomised controlled trial. BMJ Open. 2021; 11(3):e045504. [DOI:10.1136/bmjopen-2020-045504] [PMID]
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |